自1959年诺贝尔物理奖获得者理查德·费曼(Richard Feynman)在一次演讲中曾预言,人类将在原子尺度上进行物质创造。此后纳米概念便应运而生,并且逐渐在材料、环境、能源等方面大放异彩(图1),如纳米汽车、纳米衣服、抗菌材料等。

然而,除了衣食住行方面,纳米凭借“超微”结构的优势在医学领域也成为了众多科学家竞相探索的“宝藏之地”,如可以使药物精准送达病变器官甚至病变细胞的纳米输送系统。而随着近年来人们对NMN(Nicotinamide mononucleotide,β-烟酰胺单核苷酸)了解的不断深入,纳米药物输送系统是否可以运用至NMN,并进一步放大NMN本身所具有的DNA修复、提升线粒体代谢、改善心脑血管及衰老相关疾病等作用值得期待。
2021年,一篇由悉尼大学(The University of Sydney)Victoria Cogger教授(图2)等人发表在纳米技术领域顶级期刊《美国化学会-纳米》(ACS Nano)的文章,便是将一种新型纳米晶体——银量子点与NMN结合,为NMN制剂的研发打开了新视角。

该文章表明[1],当NMN附着在一种被称为“银量子点”的纳米晶体材料上后,可促肝细胞对其吸收达百倍,提升NMN效用达千倍(图3)。

NMN与银量子点
NMN是“生命必需分子”烟酰胺腺嘌呤二核苷酸(Nicotinamide adenine dinucleotide,NAD+)的直接前体,不仅可提高小鼠体内NAD+水平,还可激活一种依赖于NAD+的蛋白质(Sirtuins),从而促进新陈代谢,维持细胞能量动态平衡,延缓小鼠衰老[2]。因此,NMN近年来已逐渐被运用至抑制衰老、改善年龄相关和代谢疾病的领域。
量子点(Quantum Dot, QD)是一种多功能纳米晶体,具有生物成像、检测和药物递送的功能。理想的纳米材料转运体对人体的影响小,并在药物递送后可完全清除。然而常规量子点实际上在肝脏中会积聚而导致潜在毒性。但当银与其聚合后,可显著降低毒性,因此银量子点逐渐成为了一种理想型的药物递送载体。
基于以上NMN和量子点的特点,Cogger教授等人便着眼于将银量子点引入NMN的使用中,通过测量QD-NMN的细胞摄取率以及血液中葡萄糖的清除率,来探索该方法是否可以提高NMN的口服效果(图4)。
与NMN的结合图示.png)
首次发现银量子点是可提升NMN作用达千倍的有效载体
为了探究银量子点(QD)是否会影响NMN的作用,Cogger教授等人通过小鼠的口服葡萄糖耐量试验(oGTT),分别比较了单纯NMN和QD-NMN在不同的单剂量(仅服用一次)下对血液中葡萄糖的清除效率。
结果显示,无论是否与银量子点结合,NMN均可显著降低小鼠(3月龄)的血糖水平(图5A-B),但所用剂量有显著差别(1000倍之差),即QD-NMN仅需千分之一(1/1000)的剂量便可达到与NMN相同的效果(图5C)。此外,当同剂量时,QD-NMN(红色虚线)可相比NMN(蓝色虚线)更早的达到吸收最大值(图5D)。
为载体的NMN相比单纯NMN可更有效的发挥降血糖作用.png)
图A和B为达到同样的降血糖作用,所需的NMN和QD-NMN剂量比较;图C为不同剂量下的血糖下降程度;图D为同剂量NMN和QD-NMN达到最大下降程度的时间比较。
以上数据表明,以银量子点为载体的NMN(QD-NMN)相比单纯NMN可更有效的发挥降血糖作用。而值得注意的是,目前该领域尚未有任何关于NMN(或相关化合物,NAD+或烟酰胺核糖侧)递送的其他纳米载体方法被报道。因此,该研究首次发现银量子点是一种可提升NMN作用的有效载体。
银量子点可使剂量百倍之差的NMN达到同等吸收
上述结果发现了纳米晶体材料具有放大NMN作用的优势,接下来,Cogger教授等人继续对该作用的可能机制进行了探索。
多数纳米材料通过内吞作用被细胞吸收。因此,Cogger教授等人对比了肝细胞对单纯NMN和QD-NMN吸收机制的异同。研究分别给予小鼠单纯NMN或QD-NMN,随后对肝脏、肝细胞和肝窦内皮细胞(免疫细胞)中的总NAD和NAD+的活性,及SIRT1活性进行检测。
结果显示,800 mg/kg的NMN和8 mg/kg的QD-NMN均显著提升体内总NAD、NAD+和NADH水平,且增加趋势近似一致(图6A);其中值得注意的是,银量子点中显著促进了肝窦内皮细胞对NMN的吸收;此外,8 mg/kg的QD-NMN还可增强“长寿基因”SIRT1的活性(图6B),提示银量子点增强了肝细胞对NMN的吸收,而这可能是由于该载体改善了NMN在小肠的转运,防止肠道微生物群对其降解,从而提高了吸收量。

图A为肝脏、肝细胞、肝窦内皮细胞中总NAD、NAD+和NADH的活性变化;图B为SIRT1的活性变化,二甲双胍是一线安全可靠的降糖药,研究中用其与NMN的降糖作用进行对比。
银量子点-NMN的优势在动物长期试验中得到确证
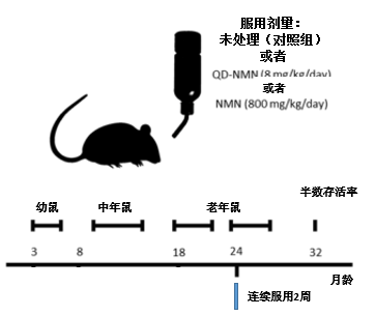
上述体内的单剂量实验发现,银量子点或许是提升NMN作用的有效载体。为了验证该结果是否在多剂量(服用多次)条件下一样有效,Cogger教授等人进行了长期的动物实验(如图7)。研究选用了24月龄的老年鼠,并连续2周服用QD-NMN(8 mg/kg/天)或NMN(800 mg/kg/天),随后对老年鼠的肝脏毒性、血糖浓度等进行了检测。
结果显示,在两周内,相比大剂量的NMN单药来说,小剂量QD-NMN便可将NAD+水平显著提高至3倍(图8A),并同时显著降低了胰岛素和胰岛素抵抗指数(图8C-D);而在肝毒性方面,QD-NMN相比NMN数值更低,说明当银量子点“加持”NMN后,可能具有效果更强,安全性更佳的优势(图8B)。
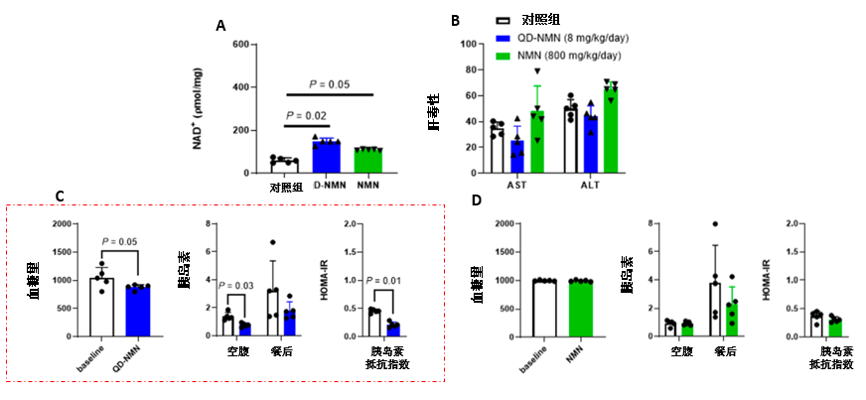
图A:体内NAD+水平变化;图B:肝毒性趋势;图C:QD-NMN的降糖作用;图D:单纯NMN的降糖作用。
NMN的临床有效性是一个越来越受关注的领域,但如何科学提高一直未有定论。而Cogger教授等人研究似乎提供了一个潜在的解题方向。数据表明,当NMN“加持”纳米科技(银量子点)后,可显著提升肝细胞对NMN的吸收,从而将NMN的益处放大百倍甚至千倍。这充分提示着,纳米科技或许是显著提高NMN作用的潜在方式。
纳米科技不仅利好医疗领域的多维度开发,在抑衰领域或许能解决众多补充剂甚至某些药物疗效不佳等问题。虽然这仍需要众多学者的努力来探索,但纳米技术或许能够将医学领域带入一种“超微时代”,从而更快、更好的实现人类健康寿命的提升。